Эѕ бр Эєвдец
еЊ вЊ ПЙОњыФЙуЗКДцдкгкздШЛНчЃЌЪЧЖЏЮяЯШЬьУтвпЕФживЊзщГЩГЩЗжЁЃPR-39ЪЧЦфжавЛРргЩ39ИіАБЛљЫсВаЛљЙЙГЩЕФЖрыФЁЃЮФеТзлЪіСЫPR-39дкНсЙЙЁЂЛљвђБэДяМАЦфЕїПиЁЂзїгУЛњРэМАЩњЮябЇЛюадЕШЗНУцЕФбаОПНјеЙЃЌВЂЖдЦфгІгУЧАОАНјааСЫеЙЭћЁЃ
ЙиМќДЪ ПЙОњыФЃЛPR-39ЃЛЛљвђБэДяЃЛзїгУЛњРэ
жаЭМЗжРрКХ S816.79
ПЙОњыФзїЮЊДцдкгкЩњЮяЬхФквЛРрОпгаЙуЦзПЙОњЛюадЕФЖрыФЃЌЪЧЫожїЗЧЬивьадЗРгљЯЕЭГЕФживЊзщГЩВПЗжЃЌдкЖЏЮяЯШЬьУтвпЛњжЦжаОпгаЬиЪтЕФвтвхЁЃФПЧАЃЌдкВИШщЖЏЮяЬхФкЗЂЯжЕФ10гржжОпгаПЙОњЛюадЕФыФРрЖМЪєгкdefensinsЃЈЗРгљЫиЃЉКЭcathelicidinsСНДѓМвзх[1]ЁЃPR-39ЪЧcathelicidinsМвзхжавЛРрИЛКЌИЌАБЫсКЭОЋАБЫсЕФЖрыФЃЌгЩ39ИіАБЛљЫсВаЛљзщГЩЃЌЗжзгСПЮЊ4 719.7DЃЌОпгаЙуЦзЕФПЙИяРМЪЯбєадКЭвѕадОњЃЌПЙецОњЕШЩњЮябЇЙІФмЁЃ
1 PR-39ЕФНсЙЙ
1.1 PR-39ЕФАБЛљЫсНсЙЙ
жэПЙОњыФPR-39гЩAgerberth[2]ЕШШЫгк1991ФъзюЯШДгжэаЁГІзщжЏжаЗжРыДПЛЏГіРДЁЃОАБЛљЫсађСаЗжЮіЃЌPR-39вЛМЖНсЙЙжаИЛКЌИЌАБЫс(Pro)ЁЂОЋАБЫсЃЈArgЃЉСНжжАБЛљЫсВаЛљЃЌЦфжа19ИіИЌАБЫсЁЂ10ИіОЋАБЫсЃЌЙЪГЦЦфЮЊPR-39ЃЈProline-arginine-richЃЉЁЃЦфгрАБЛљЫсВаЛљЗжБ№ЮЊБНБћАБЫсЁЂССАБЫсЁЂРвАБЫсЁЂвьССАБЫсКЭИЪАБЫсЃЌЦфАБЛљЫсХХСаЫГађЮЊЃКRRRPR PPYLP RPRPP PFFPP RLPPR IPPGF PPRFP PRFPЁЃдкЦфНсЙЙжаЃЌИЌАБЫсКЭОЋАБЫсЙЙГЩЕФPro-Arg-ProНсЙЙПЩФмгыЯИОњСзжЌФЄЕФЯрЛЅзїгУгаЙи[2]ЁЃОдВЖўЩЋЦзКЭИЕСЂвЖБфЛЛКьЭтЙтЦзЗжЮіЃЌPR-39дкЫЎШмвКжаВЂВЛЯёЦфЫќПЙОњыФФЧбљаЮГЩІСТна§ЛђІТелЕўЃЌЖјЪЧГЪЩьеЙадТна§ЙЙЯѓЃЌетПЩФмгыЦфИЌАБЫсКЌСПгаЙи[3]ЁЃ
1.2 PR-39ЕФЛљвђНсЙЙ
ПЙОњыФPR-39ЧАЬхЪЧвЛЬѕБрТы173ИіАБЛљЫсВаЛљЕФЛљвђЃЌЦфЛљвђНсЙЙЯрЕБНєДеЃЌНігЩ1 784bpзщГЩЃЌОпга4ИіЭтЯдзгКЭ3ИіФкКЌзгЃЈЭМ1ЃЉ[4]ЁЃЕквЛИіЭтЯдзгБэДяаХЯЂађСаЃЈPreЃЉЕФ29ИіВаЛљКЭcathelinЧАЕМВПЗж(Pro)ЕФ37ИіГЩЪьыФЃЌЭтЯдзг2КЭ3НіАќКЌcathelinЕААзаХЯЂЃЌЭтЯдзг4БрТыcathelinЕФ4ИіC-ЖЫВаЛљКЭPR-39ЕФГЩЪьыФЁЃдкPreКЭProжЎМфгавЛИіаХКХыФУИЪЖБ№ЮЛЕуЃЌПЩБЛаХКХыФУИЪЖБ№ДгЖјЧаГ§аХКХыФЁЃЖдcathelicidinПЙОњыФМвзхРДЫЕЃЌProЪЧвдвЛЖЮЗЧГЃБЃЪиЕФЧјгђЃЌАБЛљЫсЪ§ФПвЛАудк99ЁЋ114ЗЖЮЇжЎМфБфЖЏЁЃProКЭPR-39ГЩЪьыФжЎМфЛЙгавЛИівШыФУИEЃЈelastaseЃЉЕФЪЖБ№ЮЛЕуЃЌетгыPR-39ДгЯИАћФкЕФЪЭЗХВЂЗЂЛгЩњЮябЇЙІФмЯрЙиЁЃСэЭтЃЌећИіЛљвђНсЙЙжагаHindЂѓЁЂSmaЂёЁЂEcoRЂёЕШЖрИіУИЧаЮЛЕуЃЌЯдЪОСЫЖржжЯожЦадЦЌЖЯЖрЬЌадЁЃ
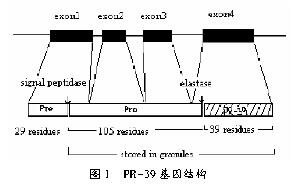
2 PR-39ЕФЛљвђБэДяМАЦфЕїПи
ДѓВПЗжcathlicidinsЕФБэДяЪЧдкЙЧЫшЯИАћЗжЛЏЕФЙ§ГЬжаНјааЕФЁЃвђДЫЃЌдкГЩЪьЕФЪШжаадСЃЯИАћжаКмФбевЕНЫќУЧЕФmRNAЁЃБрТыЕФcathlicidinsдкаХКХыФЕФв§ЕМЯТНјШыЯИАћЃЌШЛКѓаХКХыФЧаГ§ЃЌЪЃЯТЕФВПЗжНазіproformЛђепpropeptideЁЃетВПЗжЭЈГЃУЛгаПЙОњЛюадЃЌдвђПЩФмЪЧДјгавѕРызгЕФProЦЌЖЮвжжЦСЫC-ЖЫЕФбєРызгЃЌЪЙКѓепВЛФмЗЂЛгЦфЛюадЃЌЭЌЪБетвЛзїгУвВПЩвдБмУтыФЕФЯИАћФкЖОадЁЃCathlicidinsОЭвдетжжаЮЪНДЂДцдкПХСЃЬхжаЃЌЕБгаРДздЪШБНАЗПХСЃЬхЕФЕААзУИзїгУгкproformЪБЃЌЦфжаЕФПЙОњгђЦЌЖЮОЭБЛЧаИюЯТРДЃЌГЩЪьЕФПЙОњыФОЭЕУвдЗжУкЁЃећИіЙ§ГЬШчЭМ2ЫљЪОЁЃ
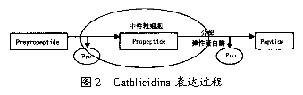
2.1 PR-39 ЕФЛљвђБэДя
Wu ЕШ1999ФъбаОПЯдЪОЃЌPR-39ЛљвђБэДягазщжЏЬивьадЁЃдкИїЩњГЄНзЖЮЃЌжэЙЧЫшжаЖМФмМьВтЕНmRNAБэДяЁЃгзСфзажэЭтжмбЊжаЪШжаадСЃЯИАћвВФмБэДяPR-39 mRNAЃЌЕЋдк42dКѓОЭМьВтВЛЕНЃЛдк4жмСфЧАЃЌзажэЕФЩіЁЂИЮКЭвЛаЉСмАЭЦїЙйЃЌАќРЈаиЯйЁЂЦЂдрКЭГІЯЕФЄСмАЭНсвВЖМФмБэДяPR-39 mRNAЃЌШЛЖј4жмСфКѓЃЌШДМьВтВЛЕНPR-39 mRNAЁЃЫцШеСфдіГЄЃЌетаЉЦїЙйКЭзщжЏжаPR-39ЛљвђБэДяЪмЕНвжжЦЃЌПЩФмЗДгГГіаТЩњзажэВЛГЩЪьЪШжаадСЃЯИАћЕФЪ§ФПБШГЩФъжэЖр[5]ЁЃ
2.2 PR-39ЛљвђБэДяЕФЕїПи
ФПЧАЕФбаОПНвЪОЃЌдкPR-39ЛљвђађСаЦєЖЏзгЧјгђгаЗЂЛгTATA boxЙІФмЕФTAAAађСаЃЌВЂЧвИУЧјгђЛЙДцдкЖрИіЧБдкЕФзЊТМЕїПивђзгЪЖБ№ЮЛЕуЃЌШчЃККЫвђзгАзНщЫи-6ЃЈNF-IL-6ЃЉЁЂАзНщЫи-6гІД№дЊМўЃЈIL-6-REЃЉЁЂSP-1ЁЂAP-2ЕШЃЌетаЉзЊТМЕїПивђзгПЩвдЕїНкPR-39ЕФЛљвђЕФБэДяЁЃWuЕШНјааСЫжЌЖрЬЧЃЈLPSЃЉЁЂАзНщЫи-6ЃЈIL-6ЃЉЁЂЪгЛЦЫсЃЈRAЃЉДІРэХрбјЕФЙЧЫшдДњЯИАћЕФЬхЭтЪЕбщЃЌМьВтетаЉЮяжЪЖджэЙЧЫшЯИАћcathelicidinПЙОњыФМвзхжаПЙОњыФPR-39КЭprotegrinБэДяЕФгАЯьЃЌгжбаОПСЫжэдкИаШОГІЕРЩГУХЪЯОњЧщПіЯТPR-39ЛљвђБэДяЧщПіЕФЬхФкЪЕбщ[6]ЁЃЬхЭтЪЕбщНсЙћЗЂЯжЃЌжЌЖрЬЧДІРэКѓЃЌPR-39 mRNAБэДяЫЎЦНЯджјЩЯЩ§ЃЌЦфЙЧЫшЯИАћХрбјЩЯЧхвКжаPR-39ХЈЖШвВЯджјдіМгЃЌБэУїLPSВЛНідкзЊТМЫЎЦНДйНјPR-39БэДяЃЌвВдкЗвыЫЎЦНДйНјЦфБэДяЃЌЖјЖреГОњЫиBдђгадіЧПLPSДйНјPR-39БэДяЕФзїгУЁЃгыДЫЯрЫЦЃЌАзНщЫи-6КЭЪгЛЦЫсвВФмгеЕМcathelicidinЛљвђЯджјБэДяЃЌдіЧПPR-39ЦєЖЏзгЃгЋЙтЫиУИБэДязгзЊШОКѓPK-15ЯИАћФкгЋЙтЫиУИЛюадЁЃЬхФкЪЕбщНсЙћЗЂЯжЃЌжэБЛИаШОЩГУХЪЯОњ6hКЭ24hКѓЃЌЦфЙЧЫшжаPR-39КЭprotegrin mRNAБэДядіМгЁЃетаЉНсЙћЖМБэУїЃЌЯИОњЃЈШчЩГУХЪЯОњЃЉЁЂЯИОњЗжНтВњЮяжЌЖрЬЧЁЂЯИАћвђзгIL-6КЭЮЂСПгЊбјЪгЛЦЫсОљФмдіЧПPR-39КЭprotegrinдкЙЧЫшдДњЯИАћжаЕФБэДяЃЌдвђМЋПЩФмОЭдкгкетаЉЮяжЪжБНгЛђМфНгМЄЛюСЫPR-39ЛљвђЦєЖЏзгЃЌДгЖјМгЧПЦфБэДяЁЃетдЄЪОСЫЭЈЙ§ЬхЭтЬэМгФГаЉЮяжЪРДЕїПиPR-39ЛљвђБэДяНЋГЩЮЊПЩФмЁЃHuawuКЭChristopherЕШбаОПЯдЪОЃЌPR-39Лљвђ5'ЖЫзЊТМЦ№ЪМЮЛЕуЧАЕк69ЁЋ63КЫмеЫсДцдквЛИіЗДЯђЕїПидЊМўЃЈnegative regulatory elementЃЉЁЃЭЈЙ§ЛљвђЕуЭЛБфНвЪОATGдкЦфжаЦ№жївЊзїгУЃЌЖјATGЪЧвЛИіЦ№ЪМУмТызгЃЌгЩДЫВТВтPR-39Лљвђ5'ЖЫзЊТМЦ№ЪМЮЛЕуЧАвЛЖЮПЊЗЂдФЖСПђМмБрТывЛжжыФЃЌВЮгыЗДЯђЕїПиPR-39ЕФБэДя[7]ЁЃ
3 PR-39ЕФзїгУЛњРэ
1993ФъBomanЕШ[8]баОПЗЂЯжPR-39ЗЂЛгПЙОњзїгУЪБВЂВЛаЮГЩПзЕРЃЌВЛСбНтЯИОњЃЌЖјЪЧЭЈЙ§вжжЦЯИАћФкDNAКЭЕААзжЪЕФКЯГЩРДЩБУ№ЯИОњЁЃБШНЯЩБОњыФ(cecropin P1)КЭPR-39ПЙДѓГІИЫОњзїгУЪБМфКѓЗЂЯжЃЌЩБОњыФФмбИЫйСбНтЯИОњЃЌЖјPR-39аш8minДЉФЄЃЌШЛКѓПьЫйЕиЩБУ№ЯИОњЃЌЖјЧвгыЩБОњыФЯрБШЃЌPR-39ЖдДІгкЖдЪ§ЩњГЄЦкЯИОњвЊБШЖдДІгкЗЧЖдЪ§ЩњГЄЦкЯИОњЕФЩБЩЫзїгУбИЫйЖјУїЯдЁЃShiЕШгУЩЈУшЕчОЕЙлВьжЄУїЃЌPR-39гыЯИАћзїгУЪБВЂУЛгадкФЄЩЯаЮГЩПзЕР[9]ЁЃФПЧАвбжЊPR-39вРППОЋАБЫсВаЛљЕФе§ЕчКЩгыЯИОњЯИАћСзжЌФЄжЎМфаЮГЩОВЕчв§СІзїгУКѓЮќИНдкЯИАћФЄЩЯЃЌШЛЖјжСгкЦфШчКЮЭИЙ§жЌжЪЫЋВуНјШыЯИАћФкЃЌДгЖјвжжЦDNAКЭЕААзжЪКЯГЩЕФШЗЧаЛњжЦЩаВЛЧхГўЁЃСэЭтЃЌPR-39ЖджаадСЃЯИАћЕФЧїЛЏзїгУЃЌМДЕїПижаадСЃЯИАћдкИаШОВПЮЛОлМЏЃЌДйНјЦфЖдВЁдЬхЕФЭЬЪЩЃЌПЩФмвВЪЧPR-39ПЙОњзїгУЕФвЛИіЗНУцЁЃ
4 PR-39ЕФЩњЮябЇЛюад
4.1 ПЙЯИОњЁЂецОњЛюад
жэПЙОњыФPR-39ЕФПЙОњзїгУжївЊЪЧеыЖдИяРМЪЯвѕадОњЃЌЖдВПЗжИяРМЪЯбєадОњвВгаПЙОњаЇЙћЁЃAgerberthЕШ[2]гУЗжРыДПЛЏЕУЕНЕФPR-39зїПЙОњЗжЮіЃЌЗЂЯжPR-39ФмУїЯдвжжЦДѓГІИЫОњЁЂЪѓЩЫКЎЩГУХЪЯОњКЭДзЫсИЦВЛЖЏИЫОњЕШ4жжИяРМЪЯвѕадОњЃЌЖдОоДѓбПцпИЫОњКЭЛЏХЇСДЧђОњвВФмВњЩњвжОњаЇЙћЃЌЖјЖдЦфЫќвЛаЉОњжъШчЦеЭЈБфаЮИЫОњЁЂЭТЬМйЕЅцпОњКЭН№ЛЦЩЋЦЯЬбЧђОњМДЪЙдк200ЁЋ300ІЬMЯТвВУЛгавжжЦзїгУ[10]ЁЃгУКЯГЩЕФPR-39зїПЙОњЪдбщЃЌвВгаРрЫЦЕФНсЙћ[4]ЃЌDelfinoЕШбаОПЗЂЯжЃЌPR-39ФмЯджјЕиНЕЕЭаТЩњаЁЪѓИаШОE. coliКѓЕФЫРЭіТЪ[11]ЁЃВЂЧвPR-39ЖдДгСйДВЗжРыЕФвЉЮяУєИаЧвОпгааэЖрФЭвЉадЕФЗЮНсКЫЗжжЇИЫОњгаПЙОњзїгУ[12ЃЌ13]ЁЃ
4.2 ЖдPMNsОпгаЧїЛЏзїгУ
Huang ЕШ[14]БЈЕРЃЌPR-39ФмгеЕМЪШжаадСЃЯИАћЕФЖЈЯђЧЈвЦЃЌЕЋЪЧЖдЕЅКЫЯИАћУЛгаЧїЛЏзїгУЃЛВЂЗЂЯжЖдЪШжаадСЃЯИАћЧїЛЏзїгУЕФНсЙЙгђПЩФмЪЧЧАЖЫЕФ26ИіАБЛљЫсЦЌЖЯЁЃдкЯИАћЭтУЛгаCa2+ДцдкЪБЃЌPR-39ВЛФмЗЂЛгЦфЧїЛЏзїгУЃЛАйШеПШЖОЫиПЩвдвжжЦЪШжаадСЃЯИАћЕФЧїЛЏзїгУКЭCa2+ЕФЖЏдБЁЃЫљвдШЯЮЊPR-39ЪЧCa2+вРРЕадЕФЪШжаадСЃЯИАћЕФЧїЛЏМСЁЃДЫзїгУвВБэУїСЫPR-39дкбзжЂЗДгІжаЗЂЛгЕФживЊзїгУ[15]ЁЃ
4.3 ДйНјЩЫПкЛжИД
PR-39ПЩвдОлМЏКЭгеЕМЯИАћБэУцЖрХфЬхОлЬЧЃЈsyndecanЃЉ-1КЭЃЈsyndecanЃЉ-4ЕФБэДяЃЌИУЬЧЪЧВЮгыВЁРэаоИДживЊЕФРрИЮЫиСђЕААзОлЬЧЁЃGallo ЕШ[16]ЪЕбщЗЂЯжЃЌPR-39дкЩЫПкДІЭЈЙ§ЯИАћЩјЭИБЛЪЭЗХЃЌШЛКѓгеЕМЖрХфЬхОлЬЧЕФБэДяВЂСбНтЯИОњЁЃPR-39ЕФПЙОњЛюадКЭгеЕМЖрХфЬхОлЬЧЛюадЪЧЗЧГЃгажњгкЩЫПкЕФЛжИДЕФЁЃ
4.4 ПЙАЉзїгУ
PR-39ФмвжжЦШЫИЮАЉЯИАћЕФШыЧжМАЧЈвЦЁЃгабаОПБэУїPR-39ПЩвдгеЕМsyndecan-1ЕФКЯГЩЃЌЖјдкШЫИЮАЉЯИАћжаsyndecan-1ЕФБэДяСПМѕЩйЃЌвђДЫЭЦВтsyndecan-1дквжжЦжзСіЯИАћЕФШыЧжКЭзЊвЦжаЗЂЛгживЊЕФзїгУЁЃOhtake ЕШ[17]баОПБэУїЃЌPR-39ОпгавжжЦШЫИЮАЉЯИАћжаМЁЖЏЕААзНсЙЙЕФИФБфКЭФмЖЏЛюадЕФЙІФмЃЌВЂЧвЛЙФмвжжЦжзСіЯИАћЕФШыЧжЃЌПЩФмЪЧвђЮЊPR-39Ждsyndecan-1гагеЕМзїгУЁЃ
4.5 МѕЛКВЁРэЫ№ЩЫ
PR-39ЭЈЙ§НсКЯp47phoxЕФSH3НсЙЙгђЃЌЧПСвЕивжжЦЭЬЪЩЯИАћNADPHбѕЛЏУИИДКЯЮяЕФзАХфЃЌЪЙЛюадбѕРрЮяжЪЃЈROSЃЉЕФВњЩњЪмЕНвжжЦЃЌДгЖјМфНгЕиМѕЧсзщжЏВЁРэЫ№ЩЫ[9,18]ЁЃзїЮЊNADPHбѕЛЏУИЕФвжжЦЮяЃЌдкРыЬхЙрзЂЪѓЗЮжаPR-39ПЩвдвжжЦгЩОжВПШБбЊКЭИпK+в§Ц№ROSЕФВњЩњ[19]ЁЃ
5 гІгУЧАОА
5.1 ШЁДњПЙЩњЫи
ЫцзХДЋЭГПЙЩњЫиЙуЗКЁЂГЄЦкЕФгІгУЃЌаэЖрВЁдОњЖдЦфВњЩњСЫФЭвЉадЁЃЖјPR-39ЕШПЙОњыФЕФПЙОњЛњжЦВЛЭЌгкДЋЭГЕФПЙЩњЫиЃЌВЛвзВњЩњФЭвЉОњжъЃЌдквНвЉвЕЩЯОпгаЙуРЋЕФЧАОАЁЃвђДЫЃЌЫцзХЖдПЙОњыФНсЙЙгыЛюадЙиЯЕМАзїгУЛњжЦЕФЩюШыбаОПЃЌНЋПЙОњыФзїЮЊПЙЩњЫиЬцДњЦЗЪЧПЩааЕФЁЃ
5.2 зЊЛљвђбаОПМАгІгУ
зажэИЙаКЁЂФЬХЃШщЗПбзМАИїжжВЁЖОадМВВЁвЛжБгАЯьаѓФСвЕЕФЗЂеЙЁЃЫцзХЗжзгЩњЮябЇМАЛљвђЙЄГЬММЪѕЕФЗЂеЙЃЌПЙОњыФЕФзЊЛљвђЙЄГЬвВШЁЕУСЫвЛаЉНјеЙЃЌЮвУЧПЩвдНшМјвбГЩЙІЕФПЙОњыФзЊЛљвђЙЄГЬЃЌШчзЊЛљвђЮУзгЁЂзЊЛљвђаЁЪѓЁЂзЊЛљвђЫЎЕОЕШЃЌАбPR-39ЕШПЙОњыФЛљвђзЊШыаѓЧнЬиЖЈЕФЯИАћШУЦфБэДяЃЌХрг§ГіПЙВЁаТЦЗжжЃЌетНЋЛсМЋДѓЕиЭЦЖЏаѓФСвЕЕФЗЂеЙЁЃ
5.3 ЫЧСЯЬэМгМСбаОП
ПЙЩњЫиЬэМгМСЕФЪЙгУбЯжиЦЦЛЕСЫЖЏЮяГІЕРЕФЮЂЩњЮяЦНКтЃЌВЂвздкЖЏЮяЬхФкВаСєЃЌбЯжигАЯьСЫаѓВњЦЗЕФЦЗжЪКЭШЫРрЕФНЁПЕЁЃПЙОњыФзїЮЊЫожїЯШЬьУтвпЗРгљжаДцдкЕФЙХРЯгжБЃЪиЕФвЛРрЕААзЗжзгЃЌОпгаЖРЬиЕФПЙОњЛњжЦЃЌШЫаѓЪГКѓвзБЛЬхФкЕФЕААзУИЫЎНтЯћЛЏЃЌЮоЖОИБзїгУЁЃвђДЫЃЌгУЛЏбЇКЯГЩЗЈКЭЛљвђЙЄГЬЕФЗНЗЈЩњВњАВШЋЁЂЛЗБЃаЭЕФPR-39ЕШПЙОњыФЫЧСЯЬэМгМСОпгаЙуРЋЕФЧАОАЁЃ
5.4 гЊбјЮяжЪЕїПиPR-39ЕФЛљвђБэДя
вбгабаОПБэУї,дкPR-39ЛљвђЕФ5ЁфЖЫЦєЖЏзгЧјгђАќКЌгаIL-6ЕШзЊТМвђзгЕФНсКЯЮЛЕу[20ЃЌ21]ЃЌНјвЛВНЫЕУїПЩвдЭЈЙ§гЊбјЮяжЪЖдЦфЛљвђБэДяНјааЕїПиЃЌДяЕНдіЧПЖЏЮяЕФЯШЬьУтвпСІЁЂЬсИпЖЏЮядчЦкПЙВЁФмСІЕФФПЕФЁЃ ВЮПМЮФЯз
1 Ramanathan BЃЌDavis EGЃЌRoss CRЃЌet alЃЎCathelicidinsЃКmicrobicidal activityЃЌmechanism of actionЃЌand roles in innate immunity[J]ЃЎMicrobes and InfectionЃЌ2002ЃЌ4(3)ЃК361ЁЋ372
2 Agerberth B, Lee JY, Bergman T, et al.Amino acid sequence of PR-39: Isolation from pig intestine of a new member of the family of proline-arginine-rich antibacterial peptides[J]. Eur.J.Biochem, 1991(202): 849ЁЋ854
3 Cabiaux V, Agerberth B, Johansson J, et al. Secondary structure and membrane interaction of PR-39, a Pro+Arg-rich antibacterial peptide[J]. Eur. J. Biochem., 1994(224): 1 019ЁЋ1 027
4 Gudmundsson G H, Magnusson K P, Chowdhary B P, et al. Structure of the Gene for Porcine Peptide Antibiotic PR-39, a Cathelin Gene Family Member: Comparative Mapping of the Locus for the Human Peptide Antibiotic FALL-39[J]. Proc. Natl Acad. Sci. USA., 1995, 92: 7 085ЁЋ7 089
5 Wu H, Zhang G, Chrestopher R, et al. Cathelicidin gene expression in procine tissues: Roles in ontogeny and tissue specificity[J]. Infection and Immunity, 1999, 67: 439ЁЋ442
6 Wu H, Zhang G, Minton J E. Regulation of cathelicidin gene expression: induction by lipopolysaccharide, interleukin-6, retinoic acid, and salmonella enterica serovar typhimurium infection[J].Infection and Immunity, 2000,68: 5 552ЁЋ5 558
7 Shimazaki K. Separation and Utilization of bovine lactoferrin[J]. Japanese Journal of Dairy and Food Science.,1989, 38: 277ЁЋ283
8 Boman H G, Agerberth B, Boman A. Mechanisms of action on Escherichia coli of cecropin P1 and PR-39, two antibacterial peptides from pig intestine[J]. Infect. Immun., 1993, 61:2 978ЁЋ2 984
9 Shi J, Ross C R, Leto T L, et al.PR-39, a proline-rich antibacterial peptide that inhibits phagocyte NADPH oxidase activity by binding to Src homology 3 domains of p47 phox[J]. Proc Natl Acad Sci USA., 1996, 93: 6 014ЁЋ6 018
10 Andrea G, Oscar C, Francosco I, et al. Antimicrobial activity of polycationic peptides[J]. Peptides, 1999, 20: 1 263ЁЋ1 273
11 Delfino D, Cusumano VV, Tomasello F, et al. Beneficial effects of antibacterial peptide PR-39 in a neonatal murine model of endotoxic shock[J]. New Microbiol, 2004, 27(4): 369ЁЋ374
12 Linde CM, Hoffner SE, Refai E, et al. In vitro activity of PR-39, a praline - arginine -rich peptide, against susceptible and multi-drug-resistant Mycobacterium tuberculosis[J]. J. Antimicrob. Chemother, 2001,47:575ЁЋ580
13 Phillip H. A. Lee, Takaaki Ohtake, Mohamed Zaiou, et al. Expression of an additional cathelicidin antimicrobial peptide protects against bacterial skin infection [J]. PNAS, 2005,102(10):3 750ЁЋ3 755
14 Huang H., Ross C.R., Blecha F. Chemoattractant properties of PR-39, a neutrophil antibacterial peptide[J].J. Leukoc. Biol. 1997,61:624ЁЋ629
15 Ramanathan B, Wu H, Ross CR, et alЃЎ PR-39, a porcine antimicrobial peptide, inhibits apoptosis: involvement of caspase-3[J]. Dev Comp Immunol, 2004,28(2):163ЁЋ169
16 Gallo R.L., Ono M., Povsic T., et al. Syndecans, cell surface heparan sulfate proteoglycans, are induced by a proline-rich antimicrobial peptide from wounds[J]. Proc. Natl Acad. Sci. USA. 1994,91:11 035ЁЋ11 039
17 Ohtake T., Fujimoto Y., Ikuta K., et al. Proline-rich antimicrobial peptide, PR-39 gene transduction altered invasive activity and actin structure in human hepatocellular carcinoma cells[J]. Br. J. Cancer, 1999,81:393ЁЋ403
18 James PE, M Madhani, Ross C, et al. Tissue hypoxia during bacterial sepsis is attenuated by PR-39, an antibacterial peptide[J]. Adv Exp Med Biol, 2003, 530: 645ЁЋ652
19 Al-Mehdi A.B., Zhao G., Dodia C., et al.Endothelial NADPH Oxidase as the source of oxidants in lungs exposed to ischemia or high K+[J]. Circ. Res. 1998,83:730ЁЋ737
20 Robert EWЃЌHancockЃЌGil DЃЎThe role of cationic anirimicrobial peptides in innate host defences[J]ЃЎTrends in MicrobiologyЃЌ2000ЃЌ8ЃК4 021
21 ЭєвдецЃЌКЋаТбрЃЌаэшїШйЃЎВИШщЖЏЮяПЙОњыФМАЦфдкаѓФСЩњВњЩЯгІгУЧАОА[J]ЃЎжаЙњаѓФСдгжОЃЌ2002ЃЌ38ЃК52
ЃЈБрМЃКеХбЇжЧЃЌЃЉ
ЭѕбрЃЌеуНДѓбЇЖЏЮяЗжзггЊбјбЇНЬг§ВПжиЕуЪЕбщЪвЃЌ310029ЃЌеуНДѓбЇЫЧСЯПЦбЇбаОПЫљЁЃ
ЭєвдецЃЌЕЅЮЛМАЭЈбЖЕижЗЭЌЕквЛзїепЁЃ
ЪеИхШеЦкЃК2006-03-27
Ёя ЙњМвЛљН№ПЮЬтЃЈNO.30571348ЃЉзЪжњЯюФП |













