РюЁЁФСЁЁЕЅАВЩНЁЁРюжйгё
еЊ вЊЁЁПЙОњыФЪЧНќФъРДЗЂЯжЕФЙуЗКДцдкгкздШЛНчжаЕФвЛРрбєРызгПЙОњЛюадыФЃЌЖрЪ§ПЙОњыФОпгаЗжзгаЁЁЂДје§ЕчЁЂСНЧзадЁЂПЙОњЦзЙуЕШЙВЭЌЬиЕуЁЃЗРгљЫиКЭCathelicidinsЪЧВИШщЖЏЮяЬхФкЕФСНДѓжївЊПЙОњыФМвзхЃЌдкВИШщЖЏЮяЕФЛњЬхЗРгљжаЦ№зХживЊЕФзїгУЁЃжэдДПЙОњыФЕФвЛАуаджЪЁЂЛљвђМАЦфБэДяЁЂдкЫожїЗРгљжаЕФзїгУЁЂзїгУЛњРэМАбаОПЧАОАНЋдкЮФжагшвдИХЪіЁЃ
ЙиМќДЪЁЁжэЃЛПЙОњыФЃЛЗРгљЫиЃЛCathelicidinsЃЛзїгУЛњжЦ
жаЭМЗжРрКХЁЁS816.79
НќФъРДЃЌгЩгквЉЮяЕФРФгУЃЌвЉЮяВаСєКЭЯИОњФЭвЉадЕШЮЪЬтШеНЅбЯжиЃЌВЛНівЛжБРЇШХзХЪРНчЕФбјжГвЕЃЌЖјЧвв§ЗЂСЫШЫУЧЖдЪГЦЗАВШЋЕФЙизЂЃЌЭЌЪБвВИјШЫРрЕФНЁПЕДјРДЧБдкЕФЭўаВЁЃдНРДдНЖрЕФЙњМвПЊЪМКєгѕНћгУПЙЩњЫиЃЌвђДЫбажЦаТвЛДњЕФПЙОњвЉЮяБуГЩЮЊвЛЯюаТЕФПЮЬтЁЃФПЧАЃЌвЛжжаТаЭЕФПЙОњвЉЮяЁЊЁЊПЙОњыФзїЮЊДЋЭГПЙЩњЫиЕФЬцДњЮявдЦфздЩэЕФЬиеїе§ЪмЕНШЫУЧЕФЙизЂЃЌОпгаЙуРЋЕФгІгУЧАОАЁЃПЙОњыФ(Antibacterial peptides)ЪЧЩњЮяЬхВњЩњЕФвЛжжОпгаПЙОњЛюадЕФЖрыФЃЌ1972ФъЃЌШ№ЕфПЦбЇМвBomanЕШЪзЯШдкЙћгЌжаЗЂЯжПЙОњыФМАЦфУтвпЙІФмЃЌЫцКѓгжДгЯЇЙХБШЬьВЯгМжагеЕМЗжРыЕУЕНЃЌГіВЂУќУћЮЊCecropinЁЃЦљНёЮЊжЙЃЌвбдкаэЖрЩњЮяжаЗЂЯж800ЖржжетбљЕФФкдДадПЙОњыФЃЌетаЉПЙОњыФГ§СЫОпгаЙуЦзЕФПЙОњЛюадЭтЃЌЭЌЪБЛЙгаИпаЇЕФПЙецОњЁЂПЙВЁЖОЁЂПЙдГцМАПЙжзСіЛюадЁЃвђДЫЃЌетаЉыФРрПЙОњЮяжЪЯдЪОСЫдквНбЇКЭХЉвЕЩЯЧБдкЕФбаОПКЭгІгУМлжЕЁЃ
1 жэдДПЙОњыФЕФжжРр
ФПЧАвбОДгжэЬхФкЗЂЯжСЫ12жжвдЩЯВЛЭЌЕФПЙОњыФЃЌ етаЉПЙОњыФОпгаВЛЭЌЕФТна§НсЙЙЃЌ ЗжзгСПЯрЖдНЯаЁЃЈаЁгк10ЁЁkDaЃЉЃЌЕЋЖдЖржжЮЂЩњЮягаЙуЦзЩБУ№зїгУЁЃИљОнПЙОњыФЧАЬхЕФЛљвђНсЙЙЁЂАБЛљЫсађСаЬиеїЃЌПЩНЋжэдДПЙОњыФЗжЮЊ4 РрЃКЗРгљЫиЃЈDefensinsЃЉГЌМвзхЁЂCathelicidinsМвзхЁЂCecropinsМвзхКЭNK-lysinЁЃCathelicidinsКЭЗРгљЫиЪЧЕНФПЧАЮЊжЙдкВИШщЖЏЮяжаЫљЗЂЯжЕФСНИізюДѓШКЬхЕФПЙОњыФМвзхЁЃ
1.1ЁЁCathelicidinsМвзх
20ЪРМЭ90ФъДњЃЌдкНјааbactenecin5 cDNAПЫТЁЪБЗЂЯжCathelicidinsгыПЙОњыФОпгаЙВЭЌЕФНсЙЙЬиеїЃЌМДNФЉЖЫЖМКЌгавЛИіCathelinЧјгђЃЌЫљвддк1995ФъНЋЦфУќУћЮЊCathelicidinsЁЃбаОПжЄУїБрТыCathelicidinsЛљвђга4ИіЭтЯдзгКЭ3ИіФкКЌзгЃЈМћЭМ1ЃЉЁЃЧА3ИіЭтЯдзгБрТыЧАЬхЧјЃЌЕк4ИіЭтЯдзгБрТыУИЧаЮЛЕуКЭПЙОњЧјгђЁЃЧАЬхЧјКЌга123ЁЋ144ИіАБЛљЫсВаЛљЃЌАќРЈвЛИі29ЁЋ30ИіВаЛљЕФаХКХыФКЭвЛИіГЄдМ94ЁЋ144ИіАБЛљЫсВаЛљЕФCathelinЧАЖЮЁЃCФЉЖЫЧјгђКЌгаГЄ12ЁЋ97ИіАБЛљЫсВаЛљЕФГЩЪьыФЖЮЁЃЧАЬхЧјОпгаИпЖШЕФЭЌдДадЃЌжэжжФкЭЌдДадДя100%ЁЃCathelinЧАЖЮЕФCЖЫЧјгђга4ИіЙЬЖЈЕФАыызАБЫсЃЌаЮГЩ2ИіЖўСђМќЁЃетаЉЛљвђЕФ5ЃЇЖЫХдВрађСаКЌгаМИИіЕїПиФЃЬхЃЌАќРЈВЮгыбзжЂЗДгІКЭМБадЦкгІД№ЕФКЫвђзг(nuclear factorЃЌNF)ЃЌШчКЫвђзгАзНщЫи-6(NF-interleukin-6)ЁЂКЫвђзгЇЌЇЃ(NF-ЇЌЇЃ)ЁЂАзНщЫи-6гІД№дЊЫиЃЈinterleukin-6 response elementЃЉЁЂМБадЦкгІД№вђзгЃЈacute phase-response factorЃЌAPRFЃЉКЭІУИЩШХЫигІД№дЊЫи(ІУ-interferon response elementsЃЌІУIRE)ЕФЮЛЕуЁЃ

CathelicidinsвдЧАыФдЕФаЮЪНДцдкЃЌЦфNЖЫЮЊаХКХыФЃЌCЖЫЪЧДјбєРызгЕФГЩЪьыФЖЮЃЌСэгаДјвѕРызгЕФCathelinЧАЖЮЃЌПЩФмгУгкжаКЭбєРызгыФЖЮЃЌЪЙЫќдкАћФкдЫЪфЁЂжќДцЪББЃГжЮоЛюадЕФЧАыФзДЬЌЃЌвдБмУтЯИАћЖОадЁЃдкЖрЪ§ЧщПіЯТЃЌетаЉПЙОњыФЕФCathelinЧјгђБЛЕААзЫЎНтУИЫЎНтЃЌЪЭЗХГівЛМЖНсЙЙИпЖШВЛЭЌЕФбєРызгПЙОњыФЁЃОЁЙмCathelicidinsЧАыФдШЗЧаЙІФмЛЙВЛЧхГўЃЌЕЋбаОПепДЇВтетаЉЗжзггаЬивьЕФЩњЮябЇЙІФмЃЌЖјВЛНіНіЪЧПЙОњыФЕФжќДцаЮЪНЁЃ
ФПЧАЃЌвбОжСЩйДг8жжВИШщЖЏЮяАќРЈжэЁЂЫЎХЃЁЂЭУЕШЬхФкЗЂЯжСЫ30ЖржжCathelicidinsЁЃжэЕФCathelicidinsМвзхАќРЈPR-39ЁЂProtegrins1ЁЋ5ЁЂPMAP-23ЃЌ36ЃЌ37ЁЃЫќУЧЖМЦ№дДгкЙЧЫшЯИАћЃЌзщГЩадЕФвдЧАыФ(Propeptides)аЮЪНДЂДцдкжмБпPMNs(жаадСЃЯИАћ)ПХСЃжаЁЃЕБPMNsМЄЛюКЭЭбПХСЃЪБЃЌФкдДадЕЏадЕААзУИАбГЩЪьыФДгЧАыФжаЧаИюГіРДЁЃдквЛаЉЧщПіЯТЃЌетаЉыФЭЈЙ§CЖЫѕЃАЗЛЏНјвЛВНаоЪЮЁЃ
1.1.1 PR-39
PR-39ЃЈproline-arginine-rich 39-amino acid peptideЃЉЪЧКЌга39ИіАБЛљЫсВаЛљЕФаЁыФЃЌЗжзгСПЮЊ4 719.7ЁЃОАБЛљЫсађСаЗжЮіЃЌЦфвЛМЖНсЙЙжаИЌАБЫсКЭОЋАБЫсНЯЖрЃЌЦфгрЮЊБНБћАБЫсЁЂССАБЫсЁЂРвАБЫсЁЂвьССАБЫсКЭИЪАБЫсЁЃИЌАБЫсКЭОЋАБЫсЙЙГЩPro-Arg-ProНсЙЙЃЌПЩФмгыЯИОњСзжЌФЄЯрЛЅзїгУгаЙиЁЃPR-39жївЊЛюадЪЧПЙИяРМЪЯвѕадОњШчДѓГІИЫОњЁЂЪѓЩЫКЎЩГУХЪЯОњЁЂТЬХЇИЫОњЕШЁЃPR-39ЛЙгаЦфЫќЕФживЊЙІФмЃЌШчЭЈЙ§НсКЯp47phoxЕФSH3НсЙЙгђЃЌЧПСвЕивжжЦЭЬЪЩЯИАћNADPHбѕЛЏУИИДКЯЮяЕФзАХфЃЌв§Ц№ЛюадбѕРрЮяжЪ(ROS)ЕФВњЩњЪмЕНвжжЦЃЌДгЖјМфНгЕиМѕЧсзщжЏВЁРэЫ№ЩЫЁЃPR-39геЕМАЉЯИАћЕФЙВЭЌНсКЯЕААзОлЬЧ-1БэДяЃЌИФБфАЉЯИАћЧжЯЎБэаЭКЭМЁЖЏЕААзНсЙЙЁЃ
1.1.2 Protegrins
ProtegrinsЛљвђНсЙЙЭЌДѓЖрЪ§CathelicidinsМвзхГЩдБвЛбљЃЌАќРЈ4ИіЭтЯдзг( E1ЁЋE4)КЭ3ИіФкКЌзгЁЃЦфжаЃЌE1ЕФвЛВПЗжБрТыPreађСаЃЌМДаХКХыФађСаЃЌЙІФмЪЧв§ЕМPropeptideНјШыЯИАћФкЃЛ E1ЕФСэвЛВПЗжКЭE2ЁЂE3МАE4ЕФвЛВПЗжвЛЦ№БрТыProађСаЃЌМДЫљгаCathelicidinsМвзхПЙОњыФжаЭЌдДадзюИпЕФВПЗж(cathlinmotif)ЃЌГЪвѕадЕФProЦЌЖЮЃЌдкЙІФмЩЯжаКЭГЩЪьЕФПЙОњыФЫљДјбєРызгЕчКЩЃЌДгЖјБЃГжPropeptideдкЯИАћФкзЊдЫЪБЮоЛюадзїгУЃЌВЂЧвБмУтЯИАћФкЖОадзїгУЃЛPeptide МДЗЂЛгВЛЭЌзїгУЕФГЩЪьыФЖЮЁЃГЩЪьЕФProtegrinsКЌга16~18ИіАБЛљЫсВаЛљЃЌвђИЛКЌCysКЭArgЖјаЏДјвЛЖЈСПЕФе§ЕчКЩЃЌвђДЫЪЧвЛжжбєРызгыФЃЈМћБэ1ЃЉЁЃProtegrinsЖМОпга2ИіЗжзгФкЖўСђМќЃЌCЖЫѕЃАЗЛЏЃЌОЖўЮЌКЫДХЙВеёЗжЮіЦфЖўМЖНсЙЙГЪІТ-елЕўЦЌЁЃProtegrinsЕФБэДяЪЧдкЙЧЫшЯИАћЗжЛЏЕФЙ§ГЬжаНјааЕФЃЌвђДЫдкГЩЪьЕФЪШжаадСЃЯИАћжаКмФбевЕНЫќУЧЕФmRNAЁЃProtegrinsЪЧЪмЕЏадЕААзУИЕїПиЕФПЙОњыФЁЃProtegrin-1ОпгаЙуЦзЕФПЙЯИОњКЭецОњЕФзїгУЃЌПЩдкЬхЭтЩБЫРКмЖрИяРМЪЯвѕадОњЃЌШчДѓГІИЫОњЁЂЭТЬМйЕЅАћОњЁЂЪѓЩЫКЎЩГУХЪЯОњКЭНсКЫИЫОњЕШЁЃHirokazuЪЕбщжЄУїЃЌProtegrin-1МАШЫЙЄКЯГЩЕФ3жжЖўСђМќЮЛжУВЛЭЌЕФвьЙЙЬхвВЖМОпгаВЛЭЌГЬЖШЕФПЙШЫРрHIV-1ВЁЖОЕФЛюадЁЃДѓСПЪЕбщЛЙБэУї,адДЋВЅЕФЩГблвТдЬхЁЂСмВЁФЮЩЊЪЯОњЁЂЕЅДП№хеюВЁЖО-2КЭСмВЁЫЋЧђОњЕШЖдProtegrinsУєИаЖШЖМКмИпЁЃ
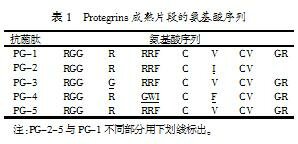
1.1.3 ЦфЫќCathelicidinsМвзхПЙОњыФ
PMAP-23ЃЌ36ЃЌ37ЃЈporcine myloid antimicrobial peptideЃЌPMAPЃЉЪєгкжэЫшдДадПЙОњыФЃЌЖдЦфНсЙЙдЄВтКЭдВЖўЩЋЦзЗжЮіБэУїPMAP-36ЃЌ37ОпгаСНЧзадІСТна§ЃЌЖјPMAP-23ГЪЗЂПЈбљНсЙЙЁЃЬхЭтЪдбщБэУїКЯГЩЕФПЙОњыФОпгаКмЧПЕФПЙОњЛюадЁЃPMAP-37ЪЧзюЧПЕФФЄЛюадвђзгЃЌдк0.2ЁЋ1ЁЁІЬmol/lЪБв§Ц№ЯИОњЯИАћФкФЄЕФЩјЭИзїгУЃЌЖјPMAP-23ЃЌ36ЕФЩБОњЛюадЗжБ№ЮЊ1ЁЋ10ЁЁІЬmol/lКЭ10ЁЋ50ЁЁІЬmol/lЁЃPMAP-37дк10ЁЋ15ЁЁІЬmol/lЪБЖдШЫЕФКьЯИАћгаШмбЊзїгУЃЌЖјPMAP-23ЃЌ36дкИпгк100ЁЁІЬmol/lЪБвВЮДЗЂЯжШмНтКьЯИАћЕФзїгУЁЃ
1.2 ЗРгљЫиМвзх
ВИШщЖЏЮяЗРгљЫиЪЧВИШщЖЏЮяФкдкЗРгљЯЕЭГзюДѓЕФГЩдБЃЌЫќЪЧвЛРрИЛКЌАыызАБЫсЕФбєРызгЛюадыФЃЌПЩаЮГЩ3ЖдЗжзгФкЖўСђМќЃЌЗжзгСПЮЊ2ЁЋ6 kDaЁЃЗРгљЫиЙуЗКБэДягкВИШщЖЏЮяЕФзщжЏЯИАћжаЃЌдкЬхЭтЃЌЮЂФІЖћХЈЖШЕФЗРгљЫиОпгаЙуЗКЕФПЙОњЛюадЃЌПЩвдЕжПЙЯИОњЁЂецОњЃЌЩѕжСвЛаЉБЛФЄВЁЖОЁЃЕБЮЂЩњЮяШыЧжЪБЃЌПЙОњыФЧАЬхЭЈЙ§ЕААзУИЫЎНтДІРэЃЌПЙОњыФКмПьБЛЪЭЗХГіРДЁЃЫќУЧЪзЯШЧжШыВЁдЮЂЩњЮяЕФДјИКЕчКЩЕФСзжЌФЄРДЗЂЛгПЙОњЙІФмЁЃИљОнАыызАБЫсЕФЮЛжУКЭЖўСђМќЕФСЌНгЃЌВИШщЖЏЮяЕФЗРгљЫиНјвЛВНПЩЗжЮЊ3ИіШКЃЌМДІСЁЂІТЁЂІШЗРгљЫиЁЃ
1.2.1 ІТ-ЗРгљЫи
ІТ-ЗРгљЫиЪЧвЛжжИЛКЌАыызАБЫсЕФбєРызгЖрыФЃЌКЌга6ИіЮШЖЈЕФАыызАБЫсЃЌЗжБ№вд1-6ЁЂ2-4ЁЂ3-5СЌНгаЮГЩШ§ИіЗжзгЕФЖўСђМќЃЌЙЙГЩЮШЖЈЕФЗДЯрЦНааЕФШ§ЙЩІТ-ЦЌВуНсЙЙЁЃЖўСђМќПЩвдЪЙаЁЗжзгЗРгљЫиНєУмСЊНсвдЗРгљЕААзУИЫЎНтЃЌЫљвддкИЛКЌЕААзУИЕФЭЬЪЩШмУИЬхЛЗОГжаШдФмБЃГжЦфЬиадЃЌетвВЪЧЗРгљЫиЧјБ№гкЦфЫќПЙЮЂЩњЮяыФЕФжївЊвђЫиЁЃжэЕФЩЯЦЄІТ-ЗРгљЫиpBD-1ЃЈporcine ІТ-defensin 1ЃЉЪЧФПЧАдкжэЬхФкЮЈвЛБЛЗЂЯжЕФЗРгљЫиЃЌpBD-1Г§ЩЯЪіНсЙЙЭтЃЌЛЙКЌга2ИіОЋАБЫсЁЂ7ИіРЕАБЫсЃЌЧвдкГЩЪьЕФыФжаВЛКЌгавѕРызгВаЛљЁЃ
ИљОнАБЛљЫсКЭКЫмеЫсађСаЕФБЃЪиадЃЌПЩНЋpBD-1ЙщРргкгеЕМБэДяаЭЁЃгУжэЩрЕФЩЯЦЄЯИАћзіХрбјЪдбщЃЌЕБгУжЌЖрЬЧЃЈLPSЃЉЁЂжзСіЛЕЫРвђзг-ІСЃЈTNF-ІСЃЉКЭАзЯИАћНщЫи-1ЃЈIL-1ЃЉДЬМЄИУЯИАћЪБЃЌpBD-1 mRNAЕФКЌСПЮоУїЯдЕФБфЛЏЃЛМьВтОЩГУХЪЯИЫОњИаШО2 dЕФЯИАћЃЌЗЂЯжpBD-1ЁЁmRNAВЂЮДдіМгЁЃетЫЕУїpBD-1ВЂВЛЪмЧАбзвђзгLPSЁЂTNF-ІСКЭАзЯИАћНщЫи-1ЕФе§ЯђЕїПиЁЃжизщЕФpBD-1ОпгаКмЧПЕФПЙОњЛюадЃЌПЩЕжПЙИяРМЪЯбєадОњЁЂвѕадОњвдМАецОњЁЃгыЦфЫќЗРгљЫиЯрЫЦЃЌpBD-1ЖдЮЂЩњЮяЕФЩБУ№ЪЧpHжЕЁЂбЮКЭбЊЧхвРРЕадЕФЃЌЕБpHжЕаЁгк5.5ЁЂИпбЮ(100ЁЋ150 mmol/l NaCl) ЛђгабЊЧхЪБЖМПЩвдЪЙжЎЪЇЛюЁЃ
1.2.2 ІС-ЗРгљЫи
ІС-ЗРгљЫизюГѕЪЧДгырЪѓКЭЭУзгЕФЖраЮКЫЪШжаадСЃЯИАћжаЗжРыГіРДЕФЃЌІС-ЗРгљЫигЩ29ЁЋ35ИіАБЛљЫсВаЛљзщГЩВЂОпга6ИіБЃЪиЕФАыызАБЫсаЮГЩЕФ3ЖдЗжзгФкЖўСђМќЃЌ3ЖдЖўСђМќЕФСЌНгЮЛжУЗжБ№ЮЊ1-6ЁЂ2-4ЁЂ3-5 СЌНгЁЃФПЧАвбДгжэЬхФкЕФЪШжаадСЃЯИАћжаЗжРыГі2жжІС-ЗРгљЫиЃЈGPDEF1ЁЂ2ЃЉЁЃЯждкЙњФкЭтЖджэЬхФкЕФІС-ЗРгљЫиБЈЕРВЛЖрЁЃ
1.2.3 ІШ-ЗРгљЫи
TangЕШЭЈЙ§ЗДЯђИпаЇвКЯрЩЋЦз(RP-HPLC) ЗЈДгтЈКяЕФАзЯИАћжаЗжРыГівЛжжГЪЛЗзДНсЙЙЕФаТаЭЕФЗРгљЫи, БЛГЦЮЊтЈКяІШаЭЗРгљЫи1(RTD-1) , УП109ИіЯИАћжаПЩЗжРыГі100 ІЬg RTD-1ЁЃ
1.3 ЦфЫќПЙОњыФМвзх
NK-lysinзюГѕДгжэаЁГІДПЛЏЕУЕНЃЌЫќКЌга78ИіАБЛљЫсВаЛљЃЌгЩTСмАЭЯИАћКЭNKЯИАћВњЩњЃЌЪЧЯИАћЖОадTЯИАћКЭNKЯИАћЕФвЛжжаТЕФаЇгІЗжзгЁЃ
Cecropin P1ЪЧЕквЛИіДгжэаЁГІжаЗжРыЕФПЙОњыФЁЃCecropin P1КЌга31ИіАБЛљЫсВаЛљЃЌЗжзгСПЪЧ3 339ЃЌВЛКЌАыызАБЫс(Cys)ЃЌВЛФмаЮГЩЗжзгФкЖўСђМќЃЌгаЧПМюадЕФNЖЫКЭЧПЪшЫЎадЕФCЖЫЃЌѕЃАЗЛЏЕФCЖЫЖдЦфЙуЦзПЙОњзїгУМЋЮЊживЊЁЃЦфАБЛљЫсађСагыРЅГцCecropinIAга64%ЯрЫЦадЃЌгыCecropinBга75%ЕФЯрЫЦадЁЃЖдЦфЖўМЖНсЙЙЕФРэТлдЄВтМАCDЦзКЭЖўЮЌКЫДХЙВеёЕФЪ§ОнЗжЮіБэУїЃЌЦфЗжзгФкКЌгаСНЧзадІС-Тна§ЃЌжаМфЪЧаЮГЩШсадЭфЧњЕФЙШАБЫс-ИЪАБЫс(Glu-Gly)ОэЧњађСаЁЃCecropinЕФПЙИяРМЪЯвѕадОњЕФЛюадвЊИпгкПЙИяРМЪЯбєадОњЕФЛюадЃЌЕЋФПЧАЛЙВЛЧхГўгЩКЮжжЯИАћВњЩњЁЃ
2 ПЙОњыФЕФзїгУЛњжЦ
ПЙОњыФЪзЯШгыВЁдЬхЯИАћФЄЕФАаВПЮЛВњЩњЯрЛЅзїгУЁЃдкетвЛЙ§ГЬжа,Ц№жївЊзїгУЕФЪЧОВЕчСІКЭЪмЬхНщЕМЕФЯИАћФЄЯрЛЅзїгУСІЁЃ
2.1 ОВЕчСІзїгУ
ПЙОњыФЕФбЁдёадгыЦфЕчадгаУмЧаЙиЯЕЃЌВЛЭЌжжРрЕФПЙОњыФОпгаЯрЕБИпЕФНсЙЙБЃЪиадЃЌВЂЧвДјгаЕчКЩЁЃЮоТлРДдДШчКЮЃЌПЙОњыФЖМФмаЮГЩСНЧзадНсЙЙЃЌдкЩњРэpHжЕЬѕМўЯТЃЌГЃДјгае§ЕчКЩЁЃЭЈГЃПЙОњыФОпгажСЩйСНИіе§ЕчКЩНсЙЙЃЌДје§ЕчКЩЕФПЙОњыФгыДјИКЕчКЩЕФЮЂЩњЮяЯИАћФЄжЎМфВњЩњЧПСвЕФОВЕчв§СІЁЃMavriЕШ(1996)ЗЂЯжЃЌаэЖрКЌгаРЕАБЫсВаЛљКЭОЋАБЫсВаЛљЕФПЙОњыФЭЈЙ§ОВЕчСІгыЯИАћФЄСзжЌЫЋЗжзгВуЕФСзжЌЛљЭХВњЩњЯрЛЅзїгУЁЃ
2.2 ЪмЬхНщЕМЕФЯИАћФЄЯрЛЅзїгУ
ПЙОњыФгыЯИАћФЄНсКЯКѓЃЌЯИАћФЄФкыФгыыФжЎМфЁЂыФгыСзжЌжЎМфЕФЯрЛЅзїгУаЮГЩвЛаЉИДдгЕФПеМфНсЙЙЃЌетаЉНсЙЙгыПЙОњыФЕФзїгУЛњРэгавЛЖЈЕФСЊЯЕЁЃыФгыыФжЎМфЕФЁЂыФгыЯИАћФЄжЎМфЕФЪшЫЎМАЧзЫЎЙІФмЧјЯрЛЅзїгУЃЌФмЪЙСНЧзадаЁыФБШЦфЫќЗНЪНИќЩюШыЯИАћФЄжааФЁЃЭЈЙ§етжжЗНЪНЙЙГЩЕФыФИДКЯЮяПЩФмаЮГЩПчФЄЭЈЕРЛђаЁПзЃЌФПЧАвбОЬсГіСЫЖржжПЙОњыФПчФЄЛњРэФЃаЭЃЌШчеЄЭАФЃаЭЁЂЛЗПзФЃаЭЁЂЬКЪНФЃаЭЁЂСНЬЌФЃаЭЕШЁЃЯпадІС-Тна§НсЙЙЕФПЙОњыФЃЈCecropinP1ЁЂPMAP-23ЃЌ36ЃЌ37ЃЉЕФПЙОњЛюадЪЧЭЈЙ§ЕиЬКЪНЛњжЦЪЕЯжЕФЃЌЖјгазХІТелЕўНсЙЙЕФЛЗыФШчpBD-1ЁЂProtegrinsЁЂNK-lysinвВаэЪЧЭЈЙ§ЭА-ЭААхЛњжЦЦ№зїгУЃЌгыДЫЛњжЦЯрЭЌЕФЛЙгаРЅГцЕФCecropinsЁЂЪШжаадСЃЯИАћЗжУкЕФІС-ЗРгљЫиЁЃСэЭтЃЌгабаОПБэУїЃЌPR-39ВЂВЛжБНгШмНтЯИОњЃЌЖјЪЧгеЕМЯИОњDNAИДжЦЫљБиашЕФЕААзНЕНтЃЌДгЖјзюКѓЩБЫРЯИОњЁЃ
ПЙОњыФЭЌЪБЗЂЛгЖржжзїгУЃЌДяЕНбИЫйгааЇЕФПЙОњЛюадЃЌетаЉзїгУВЛПЩФцЕиЦЦЛЕСЫЯИОњЕФЯИАћНсЙЙМАЙІФмЁЃОЁЙмВЛЭЌРраЭЕФПЙОњыФгЩгкРДдДЁЂзщГЩМАЙЙЯѓВЛЭЌЃЌОпгаКмДѓЕФВювьадЃЌЕЋвВгавЛаЉЙВЭЌЕФЬиеї:ЭЈЙ§ОВЕчСІЁЂЪшЫЎзїгУЕШЧзКЯСІгыАаЯИАћЯрЛЅзїгУЃЌдьГЩАаЯИАћФЄЙЙЯѓБфЛЏЁЃЕБПЙОњыФХЈЖШДяЕНвЛЖЈуажЕЪБЃЌдкЯИАћФЄЩЯаЮГЩПзОЖЛђЭЈЕРЃЌЪЙЯИАћФЄЦЦСбЃЌЯИАћФЄЦЦСбКѓЃЌжБНгЛђМфНгЕиЩЅЪЇЙІФмЃЌПЙОњыФДЉЙ§ЯИАћФЄНјШыЯИАћФкЕФАаВПЮЛЁЃ
3 ПЙОњыФЕФгІгУЧАОА
3.1 вЉгУЧАОА
ЫцзХДЋЭГПЙЩњЫиЕФЙуЗКМАГЄЦкЕФгІгУ,аэЖрВЁдДОњЖдЫќУЧВњЩњСЫФЭвЉад,ЖјОпгаЙуЦзПЙОњЧвгаЖРЬиПЙОњЛњжЦЕФПЙОњыФЯдШЛдкетЗНУцЕФгІгУбаОПжаОпгаУїЯдгХЪЦЁЃЫцзХЖдПЙОњыФНсЙЙгыЛюадЕФЙиЯЕЁЂПЙОњыФзїгУЛњжЦМАЦфЛљвђБэДяЕїПиЛњжЦШЯЪЖЕФВЛЖЯЩюЛЏ,ПЊЗЂвЛжжИпаЇЕФЁЂгаРћгкШЫРрНЁПЕЕФПЙОњыФзїПЙЩњЫиЬцДњЦЗЪЧЭъШЋПЩааЕФЁЃ
АЉжЂЪЧШЫРрМВВЁжаЕФвЛДѓФбЬт,ФПЧАЪЙгУЕФЛЏСЦвЉЮяФмЩБЫРАЉЯИАћ,ЕЋвВЭЌЪБЩБЫРШЫЬхФке§ГЃЯИАћ,ИБзїгУМЋДѓЁЃПЙОњыФФмвжжЦФГаЉжзСіЯИАћЕФЩњГЄЖјЖдШЫЬхе§ГЃЯИАћЮоКІ,етИјПЙАЉвЉЮяЕФПЊЗЂДјРДСЫЯЃЭћЁЃУРЙњЗбГЧТэИЧФўжЦвЉЙЋЫОвбгк1990ФъПЊЪМЖдЧрЭмЦЄЗєПЙОњыФ(magainin)НјааНсЙЙгыЗжзгЩшМЦ,ЩИбЁГівЛжжЖдВЁЖОКЭжзСіЯИАћОљгаЩБЩЫзїгУЕФаЁыФMA1278ЃЌФПЧАвбНјШыСйДВЂѓЦкЪЕбщЁЃ
3.2ЁЁзЊЛљвђбаОПМАгІгУ
зажэИЙаКЁЂФЬХЃШщЗПбзМАИїжжВЁЖОадМВВЁЃЌШчжэЮСЁЂМІаТГЧвпЕШвЛжБЪЧМЌЪжЕФМВВЁ,ВЛРћгкаѓФСвЕЕФЗЂеЙЁЃНшМјвбГЩЙІЕФРЅГцПЙОњыФзЊЛљвђЙЄГЬ,ШчзЊЛљвђЮУзгЁЂзЊЛљвђТэСхЪэЁЂзЊЛљвђЫЎЕОЕШ,АбЬивьЕФПЙОњыФЛљвђзЊШыаѓЧнЬиЖЈЯИАћШУЦфБэДя,ДгЖјВњЩњПЙВЁаТЦЗжж,ВЛЪЇЮЊвЛЬѕЗЂеЙаѓФСЩњВњЕФаТЫМТЗ,ЧАОАЙуРЋЁЃ
3.3ЁЁПЙОњыФЛљвђБэДяЕїПиМАПЙОњыФЬэМгМСбаОП
баОПБэУїЃЌПЙЩњЫиЬэМгМСЕФЪЙгУбЯжиЦЦЛЕСЫЖЏЮяГІЕРЕФЮЂЩњЮяЦНКт,ВЂвздкЖЏЮяЬхФкВаСє,бЯжигАЯьСЫаѓВњЦЗЕФЦЗжЪКЭШЫРрЕФНЁПЕЁЃгУЛљвђЙЄГЬЗНЗЈЩњВњЛЗБЃаЭПЙОњыФЬэМгМС,ЛђепЭЈЙ§ШеСИвђЫиЕїПиПЙОњыФЛљвђЕФБэДяЖјДяЕНаѓВњЦЗЮоПЙЩњЫиЛЏ,жЕЕУНјвЛВНбаОПЁЃ
ШЛЖј,гЩгкПЙОњыФЗжзгаЁ,ЗжРыЬсДПДцдквЛЖЈЕФРЇФб,ЙЪЬьШЛзЪдДгаЯоЁЃЛЏбЇКЯГЩКЭЛљвђЙЄГЬЗЈЛёЕУПЙОњыФЪЧжївЊЪжЖЮ,ЕЋЛЏбЇКЯГЩПЙОњыФГЩБОИп,ЖјЭЈЙ§ЛљвђЙЄГЬдкЮЂЩњЮяжажБНгБэДяПЙОњыФЛљвђ,дђПЩФмЖдЫожїгаКІЖјВЛФмЛёШЁБэДяВњЮяЁЃЫљвд,ЖдПЙОњыФЕФНсЙЙЁЂЙЙаЇЙиЯЕМАзїгУЛњРэЛЙашНјвЛВНбаОПЁЃ
ЃЈВЮПМЮФЯз35ЦЊЃЌПЏТдЃЌашепПЩКЏЫїЃЉ
ЃЈБрМЃКеХбЇжЧЃЌЃЉ
РюФСЃЌЖЋББХЉвЕДѓбЇЖЏЮягЊбјбаОПЫљЃЌ150030ЃЌЙўЖћБѕЁЃ
ЕЅАВЩНЃЈЭЈбИзїепЃЉЁЂРюжйгёЃЌЕЅЮЛМАЭЈбЖЕижЗЭЌЕквЛзїепЁЃ
ЪеИхШеЦкЃК2006-09-04 |













